যেকোনো সহজ কাজের ব্যাপারে বলতে সাধারণত বলা হয়ে থাকে, “আরে এটা তো পানির মতো সহজ”। ঠিক কী কারণে সহজকে পানির সাথে তুলনা করে এই প্রবাদের সৃষ্টি হয়েছিল তা হয়তো জানা যাবে না, কিন্তু বিজ্ঞানের দৃষ্টিতে পানি কিন্তু মোটেই সহজ বা সাধারণ কোনো পদার্থ নয়। একই রকম সমযোজী বন্ধনের সব পদার্থের থেকে পানিকে আলাদা করে রাখা হাইড্রোজেন বন্ধন, কিংবা ৪ ডিগ্রি সেলসিয়াসের আগে-পরে পানির ঘনত্বের ব্যতিক্রম ধর্ম প্রমাণ করে পানি মোটেই সাধারণ কোনো পদার্থ নয়। এখানে আলোচনা করা হবে পানিরই এক অদ্ভুত ধর্ম নিয়ে, যাকে বলা হয় এমপেম্বা ইফেক্ট (Mpemba Effect)।
এমপেম্বা ইফেক্ট কী
সাধারণভাবে বলতে গেলে ঠাণ্ডা পানির চেয়ে গরম পানির দ্রুত বরফে পরিণত হবার ঘটনাকে এমপেম্বা ইফেক্ট বলে। যেকোনো পদার্থ তরল থেকে কঠিনে পরিণত হতে দুটি ধাপ পার হতে হয়। প্রথমে তরলটি যে তাপমাত্রায় আছে সে তাপমাত্রা থেকে তার হিমাংকের (গলনাংক) তাপমাত্রায় পৌঁছবে, তারপর তাপমাত্রা পরিবর্তন না করেই সুপ্ততাপের প্রভাবে অবস্থার পরিবর্তন ঘটাবে। পানির ক্ষেত্রে ধরা যাক, ৪০ ডিগ্রি সেলসিয়াসের পানি বরফ হতে প্রথমে ৪০ ডিগ্রি থেকে শূন্য ডিগ্রিতে নামবে, তারপর শূন্য ডিগ্রিতেই পানি থেকে বরফে পরিণত হবে। এরপর তাপমাত্রা আরো কমালে বরফের তাপমাত্রা আরো কমবে।
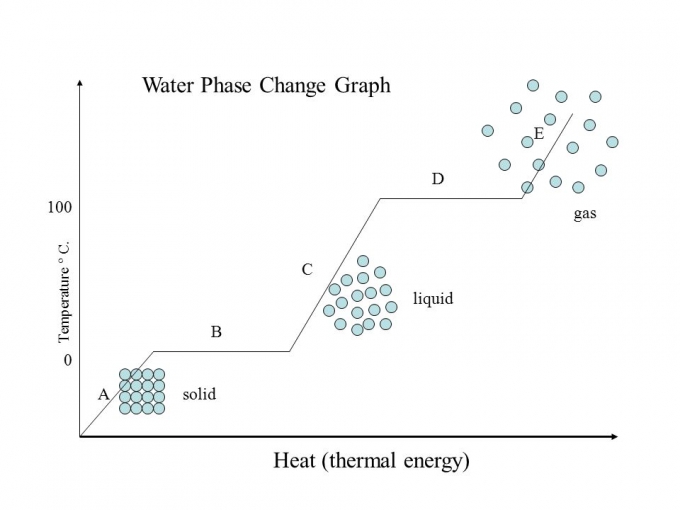
পানির বিভিন্ন অবস্থা পরিবর্তনের গ্রাফ; Source: Slide player
সুতরাং দুই গ্লাস পানির মধ্যে যে গ্লাসের পানির তাপমাত্রা শূন্য ডিগ্রির যত কাছে সেটি আগে বরফে পরিণত হবে। কিন্তু এমপেম্বা ইফেক্টে ঘটে উল্টো ঘটনা। এর প্রভাবে গরম পানি আগে বরফ হবে আর ঠান্ডা পানি হবে তার পরে! সাধারণ নিয়মের উল্টো গরম পানির দ্রুত বরফে পরিণত হবার ঘটনাকেই বলা হয় এমপেম্বা ইফেক্ট।
শুরুর কথা
১৯৬৩ সালে আফ্রিকার তানজানিয়ার ১৩ বছরের এক স্কুল বালক, এরাস্তো এমপেম্বা, যার নামে এই ইফেক্ট এর নামকরণ হয়েছে, আইসক্রিম বানাতে গিয়ে পানির এই অদ্ভুত আচরণ খেয়াল করেন। স্কুলের শিক্ষকদের তিনি এ কথা বললে তারা তার কথা বিশ্বাস করেননি। কয়েক বছর পরে হাই স্কুলে পড়ার সময় পদার্থ বিজ্ঞানের একজন প্রফেসর আসেন, ড. ডেনিস অসবর্ন, এমপেম্বা তাকে এই ব্যাপারে প্রশ্ন করেন। তার শিক্ষক আর সহপাঠীরা তাকে অবিশ্বাস করলেও ড. অসবর্নকে আগ্রহী করতে সক্ষম হন এবং ড. অসবর্ন নিজের ল্যাবে এই ব্যাপারে পরীক্ষা-নিরীক্ষা চালান। তিনি খেয়াল করেন, বাস্তবেও ঠান্ডা পানির চেয়ে গরম পানি আগে বরফে হতে পারে! তবে সেটি প্রতিবারই হয় এমন নয় বরং মাঝে মধ্যে পানির এই অদ্ভুত ধর্ম লক্ষ্য করেন তিনি। এরপর ১৯৬৯ সালে এমপেম্বা ও ড. অসবর্ন এই ব্যাপারে একটি গবেষণাপত্র প্রকাশ করেন।

এমপেম্বা ও ড. অসবর্ন; Source: The Times (Photographer: Ben Gurr)
পানির এই অদ্ভুত আচরণের বৈজ্ঞানিক ব্যাখা দেবার আগে একটু পেছনে ফিরে তাকানো দরকার। কয়েক হাজার বছর আগেই অ্যারিস্টটল পানির এই অদ্ভুত আচরণ খেয়াল করেছিলেন। তিনিই খুব সম্ভবত প্রথম এই ব্যাপারে লিখে গিয়েছেন খ্রিস্টপূর্ব ৩৫০ সালে। তার লেখা থেকে জানা যায়, পানি অনেক সময় নিয়ে গরম করলে ঠান্ডা পানির চেয়ে দ্রুত বরফ হয়ে যায়। আধুনিক যুগের বিজ্ঞানীদের মধ্যে ফ্রান্সিস বেকন পানির এই অদ্ভুত আচরণ খেয়াল করেছিলেন। বিখ্যাত গণিতবীদ রেনে ডেকার্টও, কার্টেসিয়ান স্থানাংক ব্যবস্থা যার নামে নামকরণ করা হয়েছে, পানির এই আচরণ খেয়াল করেছিলেন।
বৈজ্ঞানিক ব্যাখ্যা
প্রায় দুই-আড়াই হাজার বছর আগে থেকে মানুষ পানির এই আচরণ সম্পর্কে জানলেও আধুনিক বিজ্ঞানের চোখে পড়ে এমপেম্বা জানানোর পরেই, সঠিকভাবে বলতে গেলে ড. অসবর্নের সাথে পেপার পাবলিশ করার পরে। কিন্তু প্রায় অর্ধ শতাব্দী পার হয়ে গেলেও এখন পর্যন্ত কেউই এ ব্যাপারে কোনো পরিপূর্ণ ব্যাখা দিতে পারেননি! আর এর পেছনে রয়েছে ‘পানির বরফ হওয়া’ শব্দগুচ্ছ। পানি শূন্য ডিগ্রিতে পৌঁছালেই যে বরফে পরিণত হয় না, প্রথমে বরফের ছোট ছোট ক্রিস্টাল তৈরি হবে, তারপর সেটিকে কেন্দ্র করে পানি জমাট বাঁধবে। এখন বরফ হওয়া বলতে প্রথম ক্রিস্টাল গঠন হওয়া নাকি পুরো পানি বরফে পরিণত হওয়া সেটির কোনো সুনির্দিষ্ট সংজ্ঞা নেই।
পুরো ব্যাপারটির সুনির্দিষ্ট ব্যাখ্যা না থাকলেও এখন পর্যন্ত বেশ কয়েকটি হাইপোথিসিস আছে এ ব্যাপারে। সবচেয়ে সহজ ব্যাখা হচ্ছে পানি স্ফুটনাংকে থাকলে কিছু পানি বাষ্পীভূত হয়ে বাতাসে চলে যায়, ফলে পাত্রে থাকা পানির ভর কমে যায়। একই পরিমাণ পানি দুটি আলাদা বিকারে নিয়ে একটিকে ঘরের তাপমাত্রায় রাখা হয় আর আরেকটিকে স্ফুটনাংকের তাপমাত্রায় তাপ দেয়া হয় তাহলে তাপ দেয়াটি থেকে কিছু হলেও পানি বাষ্পীভূত হয়ে যাবে। ফলে সেই বিকারের পানির ভর একটু হলেও কমে যাবে। আর ভর কমে যাবার কারণে গরম করা পানি আগে বরফ হয়ে যায়। এই তত্ত্বের উপর ভিত্তি করে বেশ কিছু সফল পরীক্ষা হলেও তাত্ত্বিকভাবে হিসেব মেলানো সম্ভব হয় না। ফলে শুধুমাত্র ভর কমে যাওয়া একমাত্র কারণ হতে পারে কিনা তা নিয়ে যথেষ্ট সন্দেহ থেকে যায়।

বরফ ও পানি; Source: Medium
ভর কমে যাবার বাইরে আরেকটি ব্যাখ্যা পানিতে দ্রবীভূত গ্যাসের পানি থেকে বের হয়ে যাওয়া। পানিতে সবসময় বিভিন্ন গ্যাস দ্রবীভূত থাকে। যখন পানিকে গরম করা হয় তখন এসব গ্যাস ধীরে ধীরে বের হয়ে যেতে থাকে। ফলে এই গরম পানিতে ঠান্ডা পানির চেয়ে কম গ্যাস থাকে। ফলে যখন এসব গ্যাস বেরিয়ে যাচ্ছে তখন পানির হিমাংক তখন বেড়ে যাচ্ছে। উদাহরণস্বরূপ বলা যায়, পানিতে কার্বন ডাই-অক্সাইড দ্রবীভূত থাকলে পানির হিমাংক -৮ ডিগ্রী সেলসিয়াস পর্যন্ত নেমে যাতে পারে। কিন্তু কার্বন ডাই-অক্সাইডকে বের করে দিতে পারলে পরিপূর্ণ বিশুদ্ধ পানির মতো হিমাংক আবার শূন্য ডিগ্রি হয়ে যায়। ঠিক এরকমভাবেই গ্যাস বের হয়ে যাবার কারণে স্ফুটনাঙ্কের পরিবর্তন হতে পারে বলে অনেকেই মত দিয়েছেন।
২০১২ সালে রয়াল সোসাইটি অব ক্যামেস্ট্রি এক প্রতিযোগীতা আয়োজন করে এমপেম্বা ইফেক্টের ব্যাখা চেয়ে। প্রায় ২২ হাজার প্রতিযোগী তাদের ব্যাখ্যা প্রদান করে। তাদের মধ্যে নিকোলা ব্রেগোভিচকে এমপেম্বা বিজয়ী হিসেবে বেছে নেন। ব্রেগোভিচ এর আগে বলা পানির বাষ্প হওয়া আর দ্রবীভূত গ্যাসের সাথে নতুন দুটি ব্যাপারে ব্যাখ্যা করেন। একটি হচ্ছে পরিচলনের ফলে সৃষ্ট স্রোত (Convection current) এবং সুপারকুলিং। গরম পানিকে ঠান্ডা পরিবেশে রাখলে পাত্রের কিনারা দ্রুত ঠান্ডা হয়, কিন্তু মাঝের পানির তাপমাত্রা বেশি থাকে। এর ফলে ভিন্ন তাপমাত্রার পানির একটি স্রোত তৈরি হয়, যা এমপেম্বা ইফেক্টে প্রভাব ফেলে। অন্যদিকে পানি বরফ হবার আগে এর একটি অংশের তাপমাত্রা হিমাংকের নিচে নেমে যায়, সেখানে তৈরি হয় ছোট একটি ক্রিস্টাল। তাপমাত্রার এই নেমে যাওয়া হচ্ছে সুপারকুলিং, যা পানি জমাট বাঁধতে সাহায্য করে।
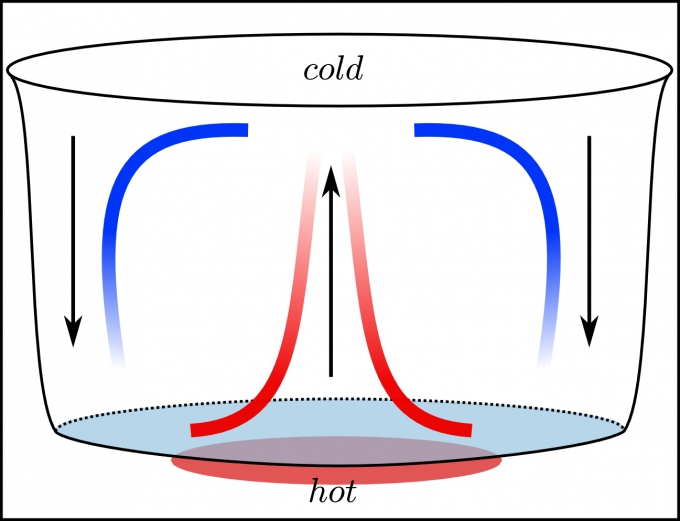
পরিচলনের জন্য সৃষ্ট একই পাত্রে ভিন্ন তাপমাত্রার পানির স্রোত; Source: MPI MIS
মজার ব্যাপার হচ্ছে, এই থিওরিও এমপেম্বা ইফেক্ট ব্যাখার জন্য পরিপূর্ণ না। কেননা কী কারণে ঠান্ডা পানির চেয়ে গরম পানির সুপারকুলিং কম হচ্ছে সেটির কোনো সন্তোষজনক উত্তর এখনো পাওয়া যায়নি। ফলে একটি রহস্যের আপাত সমাধান হলেও আরেকটি রহস্য এসে হাজির হয়ে যায়। এতক্ষণ যেগুলো বলা হলো সেগুলোর সবগুলোই একবার হলেও পরীক্ষা করে দেখা হয়েছে, কিন্তু কোনোটাকেই বিজ্ঞানীরা কারণ হিসেবে স্বীকৃতি দেননি।
সিঙ্গাপুরের নানইয়াং টেকনোলজিক্যাল ইউনিভার্সিটির জি ঝাং এবং তার গবেষক দল নতুন একটি ব্যাখা দিয়েছেন এমপেম্বা ইফেক্টের ব্যাপারে। তাদের থিওরির মূল হচ্ছে পানির ব্যতিক্রমী রাসায়নিক বন্ধন। দুটি হাইড্রোজেন আর একটি অক্সিজেন নিয়ে পানির সমযোজী বন্ধন (co-valent bond) তৈরি হয়। কিন্তু পানির সাথে এ রকম অন্যান্য যৌগের একটি বড় পার্থক্য হচ্ছে হাইড্রোজেন বন্ধন। হাইড্রোজেন বন্ধন সমযোজী বন্ধনের চেয়ে কম শক্তিশালী হলেও এই হাইড্রোজেন বন্ধনের কারণেই পানির স্ফুটনাঙ্ক বেশি হয়। জি ঝাং এর থিওরি অনুযায়ী এই হাইড্রোজেন বন্ধন পানির এই ব্যতিক্রম আচরণের জন্য দায়ী।
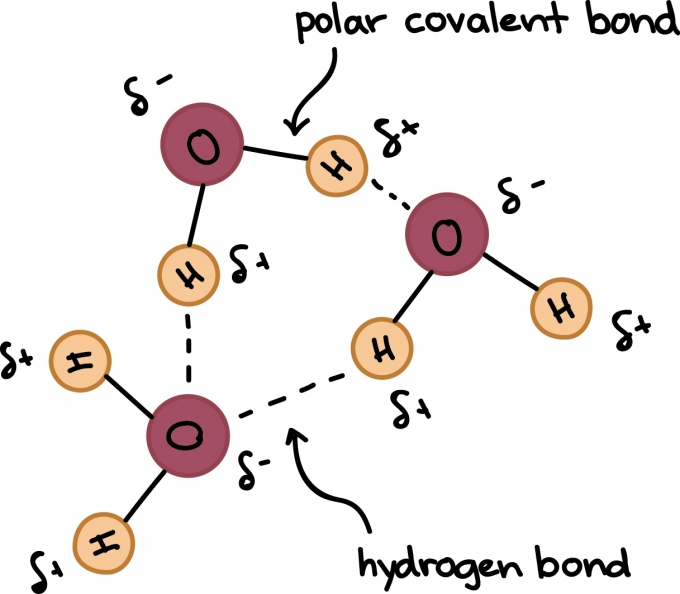
পানির রাসায়নিক বন্ধন; Source: Khan Academy
হাইড্রোজেন বন্ধন পানির অণুগুলোকে কাছাকাছি আটকে রাখে। পানিকে যখন তাপ দেয়া হবে তখন এই হাইড্রোজেন বন্ধন ধীরে ধীরে দূরে সরে যেতে শুরু করবে এবং পানির অণুগুলো একটি আরেকটি থেকে দূরে সরে যেতে থাকবে। এরপর যখন আবার ঠান্ডা করা হবে তখন হাইড্রোজেন বন্ধন আবারো আগের মতো হাইড্রোজেন অণুগুলোকে কাছাকাছি আনবে। এসময় হাইড্রোজেন বন্ধন যে এনার্জি ছেড়ে দেবে সেটাকেই গরম পানির দ্রুত বরফ হবার কারণ হিসেবে বলেছেন সিঙ্গাপুরের বিজ্ঞানীর দল। তারা তাদের থিওরি প্রমাণের জন্য গরম ও ঠান্ডা পানির Molecular activity-র একটি হিসাব দেখিয়েছেন।
তবে সব বিজ্ঞানী যে এমপেম্বা ইফেক্টের রহস্যভেদ করার জন্য কাজ করেন তা-ও না। অনেকে এটিকে কাকতালীয়ভাবে মাঝে মাঝে ঘটা একটি ঘটনা হিসেবে ব্যাখ্যা করেন। ২০১৬ সালে বুরিজ ও লিনডেন একটি গবেষণাপত্র প্রকাশ করেন, যেখানে তারা এমপেম্বা ইফেক্টকে সরাসরি অস্বীকার করেছেন। তারা বেশ কড়াভাবেই সমালোচনা করেছেন পুরো ব্যাপারটির। তাদের মতে, পরীক্ষা করার সময় পানির ভর নিতে কিংবা তাপমাত্রা পরিমাপের ভুলের কারণে মনে হতে পারে গরম পানি দ্রুত বরফ হচ্ছে। বুরিজ ও লিনডেন ছাড়াও আরো অনেকেই বেশ কিছু ব্যাপারে প্রশ্ন তুলেছেন। পানির উৎস, পানি রাখার পাত্র, তাপের উৎস, ঠান্ডা কিভাবে করা হচ্ছে- এরকম হাজারো ব্যাপার থাকতে পারে যেগুলোর কারণে হয়তো আপাতত দৃষ্টিতে একই পানি বেশি তাপমাত্রা থেকে দ্রুত বরফ হচ্ছে বলে মনে হয়। তবে যারা এমপেম্বা ইফেক্ট নিয়ে কাজ করেন তারা এখনই হাল ছেড়ে দেবার পাত্র নন বলেই জানিয়েছেন।

এমপেম্বা ইফেক্ট কী আসলেই আছে নাকি পুরোটাই ভ্রম? Source: Zidbits
প্রকৃতি সবসময় রহস্য পছন্দ করে। বিজ্ঞান অনেক দূর এগিয়ে গেলেও এখনো অনেক কিছুর পরিপূর্ণ উত্তর দিতে পারে না। কে জানে এমপেম্বা ইফেক্ট সেরকম একটি হয়েই থাকবে কিনা। সব প্রশ্নের উত্তর পেয়ে গেলে প্রশ্ন করারই আর কিছু থাকবে না। তাই কিছু রহস্য থাকা হয়ত একদিক দিয়ে ভালোই।
তথ্যসূত্র
- Tao, Yunwen; Zou, Wenli; Jia, Junteng; Li, Wei; Cremer, Dieter (2017). “Different Ways of Hydrogen Bonding in Water – Why Does Warm Water Freeze Faster than Cold Water?”. Journal of Chemical Theory and Computation. 13: 55.
- Jeng, Monwhea (2006). “Hot water can freeze faster than cold?!?”. American Journal of Physics. 74 (6): 514
- Bregović, Nikola; Mpemba effect from a viewpoint of an experimental physical chemist, 2013
- Mpemba, E. B.; Osborne, D. G. (1969). “Cool?”. Physics Education. 4 (3): 172
- H C Burridge and P F Linden, Questioning the Mpemba effect: hot water does not cool more quickly than cold Sci. Rep., 2016
ফিচার ইমেজ- Thougt Co.